شبیه سازی DNA
شبیه سازی DNA روشی است که برای تولید چندین نسخه یکسان از یک قطعه DNA در یک سلول استفاده می شود. شبیه سازی DNA به عنوان شبیه سازی ژن (gene cloning) یا شبیه سازی مولکولی (molecular cloning) نیز شناخته می شود. هر سه عبارت به جای یکدیگر برای توصیف تکنیک واحد استفاده می شوند.
DNA cloning فرصت های جدیدی را در زمینههایی مانند مهندسی ژنتیک و تحقیقات زیست پزشکی باز کردهاست. با شبیه سازی DNA، محققان می توانند عملکرد ژن را مطالعهکرده و فرآیندهای مختلف بیولوژیکی را کشف کنند.
اصل شبیه سازی DNA
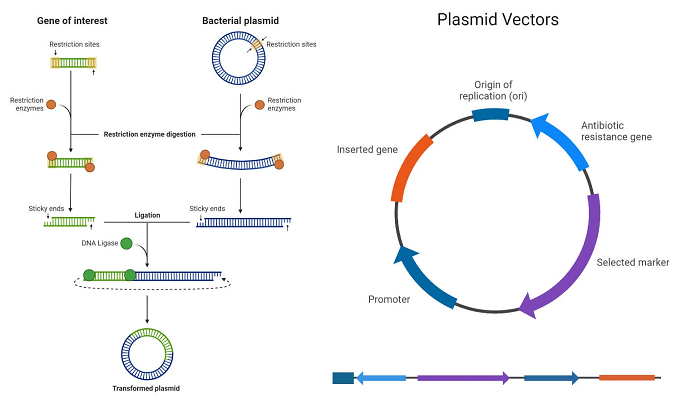
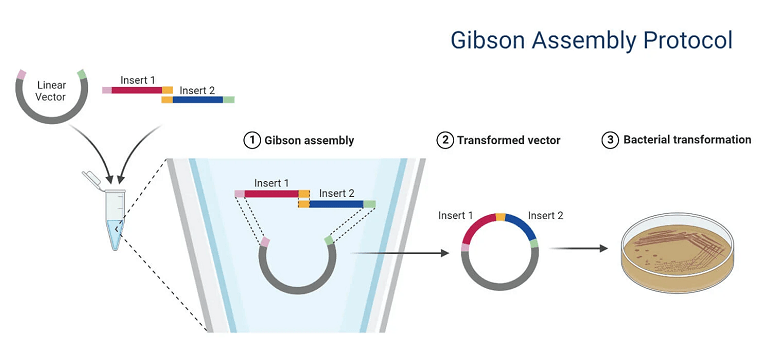
اصل شبیه سازی DNA شامل تولید چندین نسخه از یک قطعه DNA خاص موردعلاقه است. این شامل وارد کردن قطعه DNA مورد نظر در یک ناقل شبیهسازی، معمولا یک پلاسمید، برای ایجاد یک مولکول DNA نوترکیب است که سپس از طریق تبدیل (transformation) به سلول های میزبان وارد می شود. سلول های تبدیلشده انتخابشده و روی محیطهای انتخابی کشت می شوند و امکان تکثیر قطعه DNA درجشده را فراهم می کند. این منجر به تولید چندین نسخه از DNA مورد نظر می شود که می تواند برای تجزیه و تحلیل بیشتر جدا شود.
مراحل شبیه سازی DNA
فرآیند شبیه سازی DNA را می توان به پنج مرحله زیر تقسیم کرد:
1. تهیه ژن مورد نظر و ناقل
- اولین مرحله در شبیه سازی DNA بدست آوردن ژن مورد نظر است که حاوی توالی DNA مورد نظر برای شبیهسازی است.
- برای موجودات ساده مانند باکتریها، قطعه DNA را میتوان با هضم DNA ژنومی با استفاده از آنزیمهای محدودکننده بهدستآورد. موجودات پیچیدهتر، مانند پستانداران، از روشهای جایگزین مانند رونویسی معکوس mRNA یا تقویت PCR استفاده می کنند. در برخی موارد میتوان از روشهای فیزیکی مانند فراصوت یا برش برای قطعه قطعه کردن DNA استفاده کرد.
- ژن مورد نظر در یک ناقل قرار داده می شود و متداول ترین ناقل مورداستفاده پلاسمید است، یک مولکول DNA حلقوی که معمولاً در پروکاریوت ها یافت می شود.
- هم ناقل و هم ژن مورد نظر بااستفاده از آنزیم های محدودکننده یکسان یا سازگار بریده می شوند. آنزیم های محدودکننده توالی های DNA خاصی را شناسایی کرده و DNA را در آن مکان ها برش می دهند.
2. بستن ژن مورد نظر و ناقل
- پس از هضم با آنزیم های محدودکننده، ناقل و ژن مورد نظر را می توان به یکدیگر متصل کرد تا DNA نوترکیب (rDNA) را با استفاده از آنزیم DNA لیگاز تشکیل دهد.
- DNA لیگاز با شناسایی و اتصال به انتهای قطعات DNA که توسط آنزیم های محدودکننده بریده شدهاند، کار می کند. سپس تشکیل پیوندهای فسفودی استر جدید را کاتالیز می کند و به قطعات DNA می پیوندد.
3. تبدیل
- مرحله بعدی تبدیل (transformation) است که در آن rDNA به سلول میزبان وارد می شود که ژن مورد نظر درجشده را می گیرد و بیان می کند.
- قبل از تبدیل، سلولهای میزبان باید توانمند شوند، به این معنی که آنها قادر به جذب DNA از طریق غشای خود هستند.
- روشهای مختلفی برای توانمند ساختن سلولهای میزبان استفاده می شود. یک رویکرد رایج شامل استفاده از کلرید کلسیم سرد و به دنبال آن یک شوک حرارتی مختصر است.
- روش دیگر برای دستیابی به شایستگی از طریق الکتروپوریشن است. در الکتروپوریشن، سلولهای میزبان در معرض میدان الکتریکی قرار میگیرند، که منافذ موقتی در غشای سلولی ایجاد میکند و آن را برای مولکولهای DNA نفوذپذیرتر میکند.
- هنگامی که سلول های میزبان توانمند شدند، پلاسمید نوترکیب با سلول های میزبان شایسته مخلوط می شود. سپس سلول های میزبان تبدیلشده پلاسمید نوترکیب را میگیرند و آن را در مادهژنتیکی خود می گنجانند.
4. انتخاب/غربالگری و کشت سلولهای تبدیلشده
- پس از تبدیل سلول های میزبان با پلاسمید نوترکیب، مرحله بعدی انتخاب یا غربالگری سلول های تبدیلشده است.
- سلول های میزبان تبدیلشده روی یک محیط آگار مغذی که حاوی یک آنتی بیوتیک خاص است قرار می گیرند. آنتی بیوتیک بر اساس ژن مقاومت آنتی بیوتیکی موجود در پلاسمید نوترکیب انتخاب می شود.
- سلولهایی که با موفقیت تبدیل شدهاند حاوی ژنهایی با مقاومت آنتیبیوتیکی خواهند بود که به آنها اجازه رشد و تشکیل کلونی در محیطهای انتخابی را میدهد.
5. جداسازی DNA نوترکیب
- هنگامی که کلنی های سلول های تبدیلشده روی صفحه آگار تشکیل شدند، rDNA از کشت را می توان جدا کرد.
- یک کلنی منفرد از سلول های تبدیلشده از صفحه آگار انتخابشده و در یک محیط غذایی مایع کشت داده می شود.
- در طی این فرآیند، سلولهای میزبان تکثیر میشوند و پلاسمید نوترکیب، همراه با ژن مورد نظر درج شدهاش، نیز تکثیر میشوند و کپیهای متعددی از rDNA تولید میکنند.
- rDNA جداشده را می توان بیشتر مورد تجزیه و تحلیل قرار داد و برای کاربردهای مختلف مانند بیان پروتئین یا آزمایشات مهندسی ژنتیک استفادهکرد.
اجزای شبیه سازی DNA
1. وکتور شبیهسازی
2. آنزیم های محدودکننده
وکتور شبیهسازی
- وکتور یک مولکول DNA است که به عنوان یک حامل برای وارد کردن بخش خاصی از DNA خارجی به سلول میزبان برای شبیهسازی استفاده می شود.
- بهمنظوراستفاده به عنوان یک ناقل شبیهسازی، یک مولکول DNA باید ویژگی های خاصی داشتهباشد. یکی از ویژگی های مهم توانایی تکثیر در سلول میزبان است. همچنین باید کوچک باشد، معمولاً کمتر از 10 کیلو باز (کیلوبایت)، برای حمل آسان و پایداری.
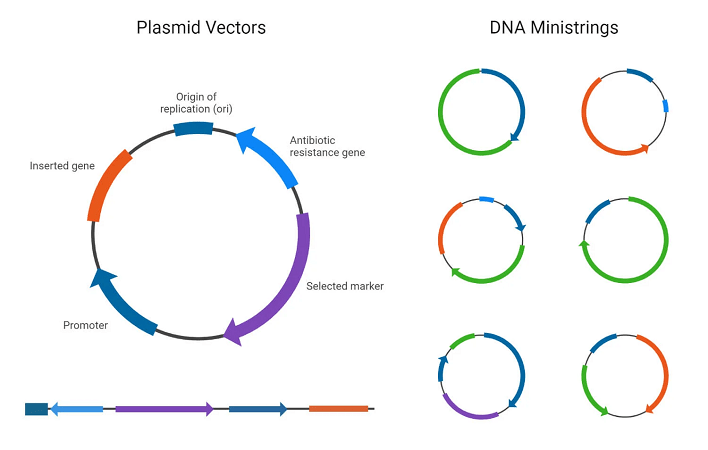
- یک وکتور همچنین به یک مکان شبیهسازی مناسب (suitable cloning site) و یک نشانگر قابل انتخاب (selectable marker) نیاز دارد که توسط آنزیم های محدودکننده خاص شناسایی شود تا قطعات DNA در وکتور وارد شود.
برخی از وکتورهای کلونینگ رایج عبارتند از:
پلاسمیدها، مولکولهای دایرهای هستند که بهطور مستقل تکثیر میشوند و بهطورگسترده بهعنوان ناقل شبیهسازی استفاده میشوند. آنها میتوانند درجهای DNA با اندازههای تا حدود 15 کیلوبایت را نگهدارند.
باکتریوفاژها که به نام فاژها نیز شناخته می شوند، ویروس هایی هستند که باکتری ها را آلوده می کنند. باکتریوفاژهایی مانند لامبدا (λ) و M13 اغلب به عنوان ناقل شبیهسازی استفاده می شوند.
کازمیدها بردارهای ترکیبی هستند که ویژگی های پلاسمیدها و باکتریوفاژها را با هم ترکیب می کنند. آنها نسبت به پلاسمیدهای معمولی پایدارتر هستند.
کروموزومهای مصنوعی باکتریایی (BACs) ناقلهای شبیهسازی بزرگی هستند که برای شبیهسازی توالیهای DNA در سلولهای باکتریایی استفاده میشوند و میتوانند بخشهای DNA تا 350 کیلوبایت را نگهدارند.
کروموزوم های مصنوعی مخمر (YACs) وکتورهایی هستند که برای شبیه سازی قطعات DNA بااندازه بزرگتر از 1 مگاباز (1 مگابایت) استفاده می شوند. آنها معمولا در نقشه برداری ژنوم و پروژههای توالییابی استفاده می شوند.
آنزیم محدودکننده
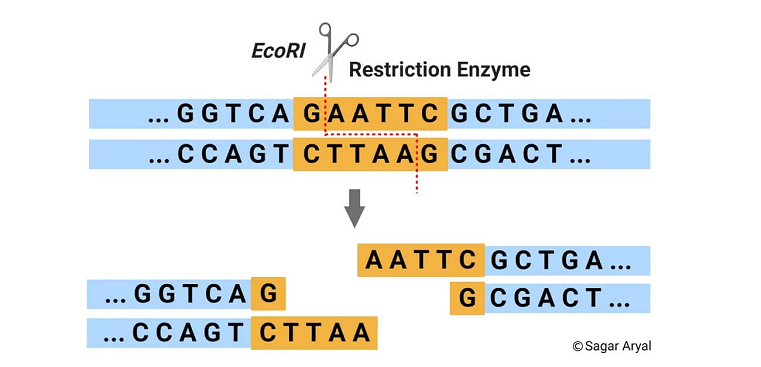
آنزیمهای محدودکننده که اندونوکلئازهای محدودکننده نیز نامیده میشوند، آنزیمهایی هستند که توسط باکتریها تولید میشوند که توالیهای DNA را در مکانهای منحصربهفردی به نام مکانهای شناسایی، شناسایی و برش میدهند.
آنزیم های محدود کننده مختلف دارای الگوهای برش متفاوتی هستند که منجر به انتهای چسبنده یا انتهای صاف می شود.
انتهای چسبنده منجر به توالیهای DNA تک رشتهای آویزان میشود که به راحتی میتوانند به سایر قطعات DNA که توسط همان آنزیم بریده میشوند، متصل شوند. از طرف دیگر، انتهای بلانت هیچ برآمدگی ندارند و برای بستن موفق به تکنیکها یا آنزیمهای اضافی نیاز دارند.
روش های شبیه سازی DNA
روش های مختلفی برای شبیه سازی DNA وجود دارد. برخی از روش های رایج شبیه سازی عبارتند از:
1. شبیهسازی سنتی
- شبیهسازی سنتی، که شبیهسازی مبتنی بر آنزیم محدود نیز نامیدهمیشود، از آنزیمهای محدودکننده برای برش DNA انتقالی و ناقل در مکانهای محدودکننده خاص استفاده میکند.
- DNA انتقالی نباید حاوی هیچ مکان محدودکننده داخلی باشد که مشابه موارد موجود در پلاسمید باشد زیرا میتواند منجر به تولید قطعات ناخواسته DNA کوچکتر شود.
- پس از برش قطعات DNA توسط آنزیمهای محدودکننده، DNA لیگاز برای پیوستن DNA انتقالی به ناقل استفاده می شود.
2. شبیهسازی PCR
- شبیهسازی PCR نوعی شبیهسازی است که شامل بستن مستقیم قطعات DNA، بهدستآمده از طریق تقویت PCR، به داخل یک ناقل بدون نیاز به برش DNA انتقالی با استفاده از آنزیمهای محدودکننده است.
- انواع مختلفی از روشهای شبیهسازی PCR وجود دارد. یکی از روش های رایج شبیهسازی PCR، شبیهسازی TA است.
- در شبیه سازی TA،آنزیم Taq پلیمراز یک باقیمانده آدنین (A) را به انتهای 3′ محصولات PCR اضافه می کند و قطعات DNA “دم A” را ایجاد می کند. این قطعات مستقیماً با وکتورهای “T-tailed” که دارای باقیمانده تیمیدین (T) در انتهای خود هستند با استفاده از DNA لیگاز متصل می شوند.
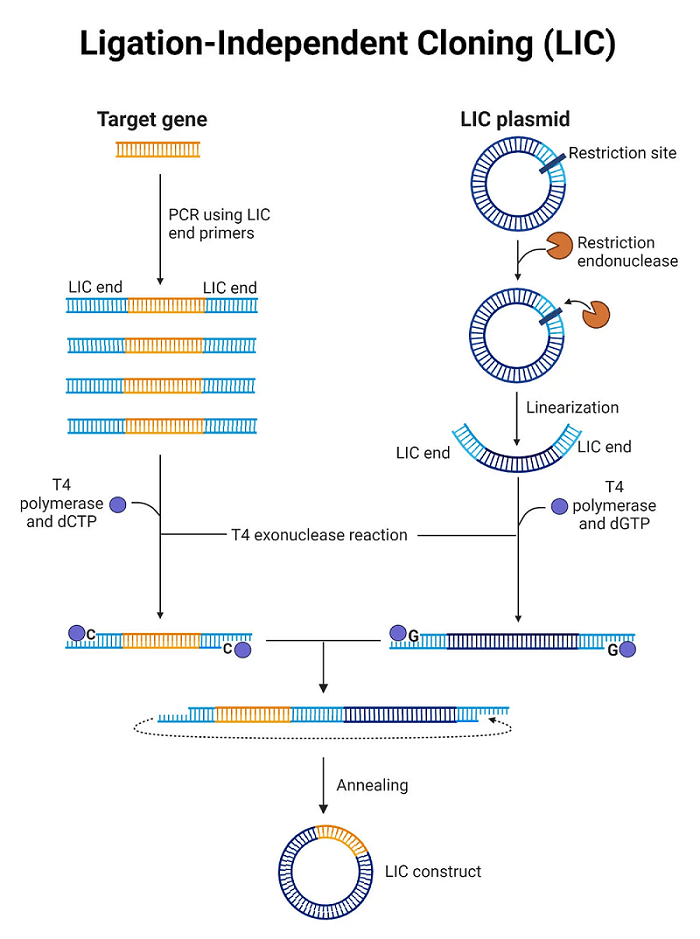
3. شبیه سازی مستقل از بستن (LIC)
- شبیهسازی مستقل از بستن (LIC) روشی است که در آن توالیهای کوتاه خاصی به انتهای یک DNA انتقالی اضافه میشوند تا با توالیهای روی یک وکتور مطابقت داشته باشند.
- انتهای 3 پریم قطعه DNA با استفاده از آنزیم هایی با فعالیت اگزونوکلئاز 3پریم به 5پریم بریده می شود که انتهای چسبنده بین DNA انتقالی و ناقل ایجاد می کند.
- مولکول های وکتور و انتقالی با هم ترکیب می شوند. پلاسمید حاصل شامل چهار شیار DNA تک رشتهای است که توسط میزبان در طول تبدیل ترمیم می شود.
4. شبیه سازی بدون درز (SC)
- شبیه سازی بدون درز (SC) روشی است که بر تطبیق توالی های کوتاه در انتهای یک قطعه DNA با توالی های کوتاه متناظر بر روی یک وکتور متکی است. شبیه به روش LIC است.
- در SC، آنزیمی با فعالیت اگزونوکلئاز 5 پریم به 3 پریم برای ایجاد اورهانگ 3 پریم بر روی قطعه DNA استفاده می شود.
- مزیت Seamless cloning نسبت به شبیه سازی سنتی این است که امکان درج چند قطعه DNA را در یک ناقل فراهم می کند.
5. شبیه سازی نوترکیبی
- شبیه سازی نوترکیبی شامل استفاده از DNA recombinases اختصاصی سایت است که تبادل و نوترکیب قطعات DNA را در مکان های نوترکیبی خاص تسهیل می کند.
- این فرآیند با وارد کردن یک قطعه DNA در یک ناقل ورودی و ایجاد یک کلون ورودی آغاز می شود. هنگامی که کلون ورودی به دست آمد، با یک کلون مقصد دوباره ترکیب می شود.
- شبیهسازی نوترکیبی مسیر کارآمدی برای ایجاد ساختارهایپیچیده DNA با امکان انتقال آسان قطعات DNA بین وکتورهای مختلف از طریق نوترکیبی خاص سایت فراهم می کند.
کاربردهای شبیه سازی DNA
DNA کلونینگ کاربردهای زیادی در زمینه های مختلف تحقیقاتی دارد. برخی از کاربردهای اصلی همراه با نمونه هایی از شبیه سازی DNA عبارتند از:
- شبیه سازی DNA برای مطالعه عملکرد ژنی ژن های خاص در موجودات مختلف مفید است. به عنوان مثال، شبیه سازی ژن پروتئین فلورسنت سبز (GFP) از چتر دریایی امکان تجسم بیان پروتئین در سلول های زنده را فراهم کرده است.
- شبیه سازی DNA برای تولید پروتئین های نوترکیب در مقادیر زیاد استفاده شده است. برای مثال، شبیهسازی ژن انسولین انسانی منجر به تولید انسولین در مقیاس بزرگ برای درمان دیابت شد و وابستگی به انسولین مشتقشده از حیوان را کاهش داد.
- شبیهسازی DNA نقش مهمی در مهندسی ژنتیک برای ایجاد ارگانیسمهای اصلاحشده ژنتیکی (GMOs) ایفا میکند که ژنهای مورد نظر را به ارگانیسمها معرفی میکند تا صفات آنها را اصلاح کنند. بهعنوان مثال، شبیهسازی ژنها برای ایجاد محصولات اصلاحشده ژنتیکی با ویژگیهای بهبودیافته مانند مقاومت به آفات و عملکرد بالاتر.
- شبیه سازی DNA در ژن درمانی نیز مفید است، جایی که ژن های درمانی شبیه سازی شده و برای درمان بیماری های ژنتیکی استفاده می شود.
- تکنیک های شبیه سازی DNA نیز در تجزیه و تحلیل پزشکی قانونی استفاده می شود. شبیه سازی مناطق خاص DNA می تواند در تقویت و تجزیه و تحلیل نشانگرهای ژنتیکی برای تعیین هویت فرد در تحقیقات پزشکی قانونی استفاده شود.
چالش ها و محدودیت های شبیه سازی DNA
شبیه سازی DNA پیشرفت های قابل توجهی در زمینه های مختلف داشته است، اما محدودیت هایی نیز دارد که باید در نظر گرفته شود. برخی از چالش ها و محدودیت ها عبارتند از:
- شبیه سازی DNA سنتی می تواند زمان بر باشد، به خصوص زمانی که با قطعات بزرگ DNA کار می کنید. ممکن است چندین روز طول بکشد تا مراحلی مانند کشت و هضم محدود انجام شود.
- محدودیت دیگر احتمال آلودگی در طول فرآیند شبیهسازی است.
- شبیه سازی DNA به دلیل معرف ها، آنزیم ها و تجهیزات مورد نیاز می تواند پرهزینه و کار فشرده باشد.
- برای اطمینان از شبیهسازی موفق، سازگاری بین DNA انتقالی و وکتور باید در نظر گرفتهشود.
ملاحظات اخلاقی در شبیه سازی DNA
شبیه سازی DNA چندین نگرانی اخلاقی را ایجاد می کند. برای اطمینان از شیوههای اخلاقی در شبیه سازی DNA، پرداختن و در نظر گرفتن این نگرانی ها و ملاحظات اخلاقی مهم است.
یکی از نگرانی ها، اصلاح ژنتیکی است که سوالاتی را در مورد پیامدهای بالقوه برای موجودات و اکوسیستم ها ایجاد می کند.
معرفی ارگانیسم های کلونشده یا اصلاحشده ژنتیکی (GMOs) به محیط می تواند اثرات زیست محیطی ناخواستهای داشتهباشد که نیاز به ارزیابی دقیق دارد.
موضوع اخلاقی دیگر، ثبت اختراع و تجاری سازی منابع ژنتیکی است که ممکن است بر تحقیقات علمی و دسترسی به اطلاعات ژنتیکی تأثیر منفی بگذارد.
حفظ حریم خصوصی اطلاعات ژنتیکی نیز با نگرانی در مورد محرمانه بودن و سوء استفاده احتمالی از دادههای ژنتیکی افراد، یک نکته مهم است. هنگامی که افراد انسانی در تحقیقات شبیهسازی مشارکت دارند، رضایت آگاهانه نیز بسیار مهم است.
درحال حاضر مجموعه کیمیا زیست گستر نوین قادر به ارائه انواع مواد اولیه با گریدهای غذایی، دارویی، آرایشی، بهداشتی و صنعتی در حجم های بالا و کیفیت عالی از تولید کننده های معتبر می باشد. درصورت نیاز می توانید درخواست خود را با ما درمیان گذاشته تا در سریعترین زمان ممکن اطلاعات لازم را در اختیارتان قرار دهیم.